Progetti di ricerca
“Dalla regolazione dell’RNA alla funzione mitocondriale: i progetti in corso del nostro laboratorio.”
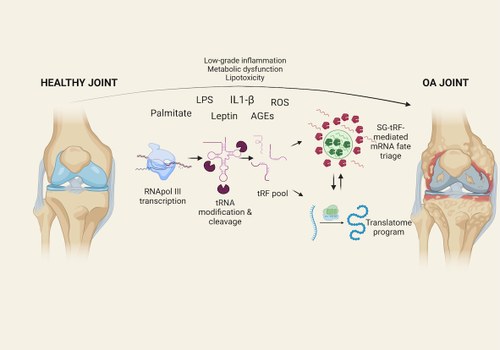
tRNA-derived fragments e microRNA: regolatori multi-layer del destino cellulare
Al MoBiDD Lab esploriamo l’affascinante universo dei tRNA-derived fragments (tRFs) e dei microRNA (miRNA) — piccole ma cruciali molecole di RNA che regolano l’espressione genica su diversi livelli post-trascrizionali. Lungi dall’essere semplici sottoprodotti del processamento dell’RNA, questi frammenti agiscono come regolatori multilivello, modulando la stabilità e la traduzione degli mRNA, nonché funzioni mitocondriali ed epigenetiche.
Quando la loro espressione viene alterata, l’equilibrio cellulare si rompe, innescando stress, infiammazione e processi degenerativi.
Attraverso l’impiego di tecnologie NGS (Next Generation Sequencing) all’avanguardia e di analisi bioinformatiche avanzate, il nostro gruppo indaga come la deregolazione di tRFs e miRNA contribuisca all’insorgenza e alla progressione di malattie degenerative come l’osteoartrite (OA) in collaborazione con l’Istituto Ortopedico Rizzoli. L’obiettivo finale è identificare nuovi target molecolari e sviluppare strategie terapeutiche basate sull’RNA per ripristinare l’omeostasi cellulare e contrastare la degenerazione tissutale.
In collaborazione con:
-Dr. Cristina Cosentino, Prof. Romano Regazzi (University of Lausanne, CH)
-Dr. Rosa Maria Borzì (IRCCS-Istituto Ortopedico Rizzoli, ITALY)
-Dr. Martin Lotz (TSRI, La Jolla, CAL, USA)
CONTATTO: Stefania D'Adamo stefania.dadamo2@unibo.it

Estratti algali ad uso fitoiatrico e fitoterapico, in agricoltura biologica e nella salute umana
Il progetto Extrafit esplora il potenziale degli estratti algali e dei loro derivati come risorse naturali per la protezione e la salute delle piante e dell’uomo.
Nato con l’obiettivo di sviluppare bioattivi eco-sostenibili, il progetto indaga l’impiego di specie algali come Jania adhaerens e Arthrospira platensis (spirulina) per il biopriming dei semi, in particolare di pomodoro, al fine di migliorare la resistenza a stress abiotici e patogeni fungini.
Oltre agli effetti fitosanitari e biostimolanti, il MoBiDD Lab contribuisce allo studio delle potenzialità fitoterapiche di questi estratti in modelli cardiovascolari e osteoarticolari, valutandone l’azione citoprotettiva, antiossidante e anti-infiammatoria.
Grazie a un approccio integrato di biochimica e biologia molecolare, il progetto mira a identificare nuovi bersagli cellulari e molecolari, promuovendo un utilizzo terapeutico e preventivo dei derivati algali e valorizzando il loro impiego in un’ottica di economia circolare e sostenibilità ambientale.
In collaborazione con:
- Prof. Roberta Roberti, DISTAL, UniBO
- Dr. Stefania Galletti, CREA, ITALY
CONTATTO: Silvia Cetrullo silvia.cetrullo@unibo.it
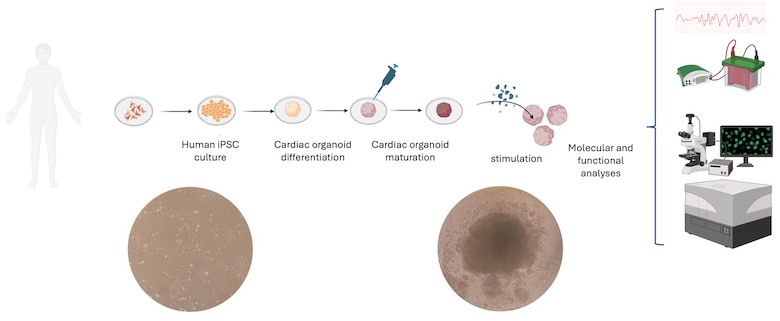
Organoidi Cardiaci e Biomarcatori Predittivi per la Medicina Personalizzata nello Scompenso Cardiaco
Al MoBiDD Lab, ci dedichiamo allo sviluppo di modelli di studio in vitro come organoidi cardiaci derivati da cellule staminali pluripotenti indotte (iPSC), con l’obiettivo di analizzare in profondità i meccanismi cellulari e molecolari alla base dell’heart failure (HF). Questi mini-cuori riproducono in vitro la complessità del tessuto miocardico umano, consentendo di studiare in modo realistico la contrattilità, il rimodellamento tissutale e le alterazioni metaboliche associate alle diverse forme di scompenso cardiaco.
Parallelamente, conduciamo studi sui microRNA circolanti (miRNA) isolati dal siero di pazienti con HFpEF (heart failure con frazione di eiezione preservata), con l’obiettivo di identificare firme molecolari utili alla stratificazione dei pazienti e alla previsione della progressione clinica.
Attraverso l’impiego di approcci di machine learning, integriamo dati molecolari e clinici per identificare biomarcatori predittivi e nuovi target terapeutici, aprendo la strada a interventi più mirati ed efficaci. L’integrazione tra modelli organoidi avanzati e analisi computazionali rappresenta un passo decisivo verso una medicina personalizzata e predittiva, trasformando lo studio dello scompenso cardiaco da osservazione a strategia di intervento.
In collaborazione con:
Istituto Nazionale per le Ricerche Cardiovascolari
CONTATTO: Silvia Cetrullo silvia.cetrullo@unibo.it
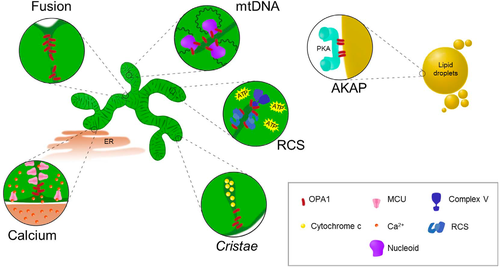
Dinamica mitocondriale e neurodegenerazioni
La dinamica mitocondriale regola la morfologia, il numero e la qualità dei mitocondri attraverso fusione, fissione, biogenesi e mitofagia, processi essenziali per la produzione energetica e l’omeostasi cellulare. Tra le proteine coinvolte, OPA1, una GTPasi della famiglia delle dinamine, svolge un ruolo chiave nella fusione mitocondriale, nell’organizzazione delle cristae, nella stabilità del DNA mitocondriale (mtDNA) e nell’efficienza della fosforilazione ossidativa (OXPHOS). Nell’uomo esistono otto isoforme di OPA1, specifiche per tessuto. Le mutazioni di OPA1 rappresentano la principale causa di atrofia ottica dominante (DOA) e della forma sindromica DOA plus, ma sono anche implicate in un più ampio spettro di neurodegenerazioni mitocondriali (Parkinson, Alzheimer, sclerosi multipla, CPEO, miopatie mitocondriali).
L’obiettivo del progetto è analizzare i meccanismi cellulari e molecolari alla base delle neurodegenerazioni causate da mutazioni di OPA1 ed identificare molecole terapeutiche in grado di ripristinare la funzionalità mitocondriale.
Attualmente non esistono terapie risolutive, ma un approccio di drug repurposing ha portato all’identificazione di sei composti (OPA1 rescuing molecules, ORMs), approvati dalla FDA, capaci di migliorare le funzioni energetiche, aumentare i livelli di OPA1 e mtDNA, e ridurre lo stress ossidativo in modelli cellulari umani (fibroblasti derivati da pazienti) e murini (fibroblasti embrionali di topo con il knockout di OPA1 murino e l’espressione di OPA1 umana wild-type e mutata).
Questi risultati propongono OPA1 come nuovo target terapeutico e gli ORMs come potenziali candidati farmacologici per il trattamento o la prevenzione delle neurodegenerazioni mitocondriali legate a mutazioni di OPA1, rapidamente trasferibili alla sperimentazione clinica.
In collaborazione con:
Dott.ssa Alessandra Maresca e Prof. Carelli, IRCCS Istituto delle Scienze Neurologiche di Bologna,
Prof.ssa. Anna Maria Ghelli e Prof. Francesco Musiani, FABIT, UNIBO.
CONTATTO: Claudia Zanna claudia.zanna@unibo.it